Biologická filtrace označuje bakteriální přeměnu organických dusíkatých sloučenin na dusičnany.
Kroky v tomto procesu jsou souhrnně známé jako cyklus dusíku. Ačkoli cyklus dusíku začíná přeměnou organických sloučenin obsahujících dusík na amoniak, je žádoucí, aby první stupeň byl dokončen před vstupem materiálu do biologického filtru. Hlavním účelem biologického filtru je přeměnit amoniak na dusitany a dusitany na dusičnany. Tyto reakce jsou velmi důležité, když je umělá nádrž osazena rybami, protože amoniak je vysoce toxický metabolický produkt přímo uvolňovaný mnoha vodními organismy a vedlejší produkt životně důležité činnosti mnoha bakterií. Dusitany jsou o něco méně toxické než amoniak ve formě NH3, i když pro některé druhy jsou toxické v koncentracích nižších než 2.5 mg/l. Dusičnany jsou považovány za relativně netoxické pro většinu vodních organismů.
Biologické filtrační zařízení pro umělou nádrž.
Biologický filtr je obvykle porézní pevná vrstva, která obsahuje nitrifikační bakterie. Bakterie získávají potřebné živiny a kyslík z vody protékající filtrační vrstvou. Jednoduchý biologický filtr je krabice naplněná štěrkem. Voda vstupuje shora, protéká filtrační vrstvou a vytéká drenážním potrubím ve spodní části boxu.

Rýže. 1. Jednoduchý biologický filtr směrem dolů.
Existuje několik typů biologických filtrů:
- Ponorné filtry (jako filtr zobrazený na obr. 1) jsou filtry, u kterých je filtrační vrstva zcela ponořena ve vodě. Ponorné filtry se v závislosti na směru proudění vody dělí na směřující dolů a nahoru. Ve filtru směřujícím dolů voda vstupuje shora a vytéká zespodu, zatímco ve filtru směřujícím nahoru je proud vody směrován zdola nahoru. Někdy se používají i ponorné filtry s horizontálním průtokem vody.
- Skrápěcí filtry jsou biologické filtry, ve kterých je hladina vody udržována pod dnem filtru. Voda vstupuje shora a vytváří vodní film na povrchu pevné fáze, ale nevyplňuje póry mezi částicemi filtrační vrstvy. To zajišťuje proudění vody směrem dolů a přirozené provzdušňování, když vzduch prochází filtrem.
Nejúčinnější jsou vzestupné ponorné a skrápěcí filtry. U skrápěcích filtrů je přívod kyslíku zajištěn přirozenou konvekcí vzduchu a filtry se ucpávají pevnými látkami. Dobu zdržení však lze upravit pouze zvýšením tloušťky filtrační vrstvy. U filtrů zaplavených směrem nahoru je méně pravděpodobné, že se zanesou pevnými látkami než u jiných ponorných filtrů. Umožňují také nastavit retenční čas v širokém rozsahu změnou průtoku vody.
Procesy probíhající v biologickém filtru pro umělou nádrž.
Nitrifikace je dvoustupňový proces přeměny amonia (NH+ 4) na dusitany (NO – 2), a dusitany na dusičnany (NO – 3). První fázi tohoto procesu (přeměna amonia na dusitany) provádějí autotrofní bakterie rodu Nitrosomonas, které jsou schopny v přítomnosti kyslíku oxidovat amonium na dusitany, přičemž jako energii využívají přibližně 270 kJ/mol. zdroj.
Ve druhém stupni procesu nitrifikace se při oxidaci dusitanů na dusičnany uvolňuje přibližně 73 kJ/mol. Tuto reakci provádějí bakterie rodu Nitrobacter, které uvolněnou energii využívají k metabolickým procesům.
Reakce přeměny amonia na dusitany a dusitany na dusičnany vyžadují značné množství kyslíku. Stechiometrická potřeba kyslíku pro přeměnu amonia na dusitany je 3,43 kg kyslíku na 1 kg oxidovaného amonia. Přeměna dusitanů na dusičnany vyžaduje 1,14 kg kyslíku na 1 kg oxidovaného dusitanu. Přeměna 1 kg amonia na dusičnan tedy vyžaduje 4,57 kg kyslíku. Vzhledem k tomu, že biologický filtr vyžaduje ke svému provozu alespoň stechiometrické množství kyslíku, přívod kyslíku se může stát faktorem omezujícím nitrifikační procesy probíhající v biofiltru.
Chemické procesy konverze amonium-dusitan-dusičnan jsou používány bakteriemi Nifrosomonas a Nitrobacter k výrobě energie. Bakterie využívají tuto energii, oxid uhličitý a kyslík k produkci organických sloučenin nezbytných pro buněčný růst a metabolismus. Pro biologické filtry má velký význam objem buněčné hmoty tvořené rostoucími bakteriemi, protože umírající bakterie tvoří částice suspendované ve vodě, které ucpávají filtr, což vede k tvorbě anaerobních oblastí v něm, velké tlakové ztráty vody protékající filtrem a další nežádoucí důsledky.
Při oxidaci 1 kg amonia na dusičnan vznikne 147 g buněk Nitrosomonas a 20 g buněk Nitrobacter. Naštěstí ve srovnání s heterotrofními bakteriemi nitrifikační bakterie produkují malou masu buněk na hmotnost oxidovaného substrátu a v důsledku toho se filtry tolik nezanášejí, pokud je množství organické hmoty vstupující do nitrifikačního filtru omezeno na minimum. Oxid uhličitý (C0) se podílí na syntéze buněk autotrofních organismů.2). Oxid uhličitý částečně uspokojuje potřebu kyslíku a je také zdrojem uhlíku.
Bakterie Nitrosomonas spotřebuje 3,02 kg kyslíku na každý kilogram amonia oxidovaného na dusitany a Nitrobacter spotřebuje 1,02 kg kyslíku na kilogram dusitanu oxidovaného na dusičnany. Celková spotřeba kyslíku je tedy 4,04 kg na kilogram amonia oxidovaného na dusičnan. Protože však tento poměr závisí na stáří plodiny, množství kyslíku potřebné k úplné oxidaci 1 kg amonia na dusičnany se pohybuje od 4 do 4,6 kg.
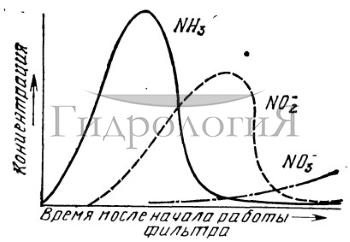
Rýže. 2. Nitrifikační křivky.
Na Obr. Obrázek 2 ukazuje vztah mezi obsahem amoniaku, dusitanů a dusičnanů v počáteční fázi provozu biologického filtru. Na začátku provozu je populace nitrifikačních bakterií buď malá, nebo chybí, takže přidání ryb do systému rychle zvýší koncentraci čpavku ve vodě. Tento bod je kritický, protože i nízké koncentrace amoniaku mohou být škodlivé pro kulturní organismy. Pokles koncentrace amoniaku obvykle signalizuje vznik odolné populace Nitrosomonas, která přeměňuje amoniak na dusitany. Takový předpoklad však může vést k nebezpečnému uspokojení. Biologický filtr obvykle obsahuje jak heterotrofní, tak autotrofní (nitrifikační) bakterie. Heterotrofní bakterie se vyznačují zrychlenou dobou generování (tj. dobou růstu, reprodukce a produkce velké populace) než autotrofní bakterie – tedy heterotrofní bakterie, které využívají zdroj jednoduchého organického uhlíku, ale pro metabolismus potřebují anorganický dusík, zpočátku stát se dominantním ve filtru a využívat amoniak produkovaný v systému. Snížení obsahu organického uhlíku potlačuje růst heterotrofních bakterií. Počáteční pokles koncentrace amoniaku proto nemusí ukazovat na nitrifikaci, ale spíše na přítomnost velké populace heterotrofních bakterií. Naštěstí to není v akvakultuře často pozorováno.
Nárůst populace Nitrosomonas vede ke zvýšení koncentrací dusitanů, které dosahují maxima a poté začínají klesat, jak roste populace Nitrobacter, přeměňuje dusitany na dusičnany. Nebezpečné jsou také zvýšené koncentrace dusitanů, protože jsou toxické pro ryby a mnoho dalších vodních organismů. Systematické sledování koncentrací dusitanů a amoniaku umožňuje zajistit, že probíhá nitrifikace.
V každém vodném systému je amoniak přítomen ve formě NH + 4 a NH3, protože mezi těmito dvěma formami je ve vodě rovnováha. Neiontová forma amoniaku (NH3) je toxický pro většinu vodních organismů v koncentracích 1 mg/l a nižších. Zvláště citlivé na NH3 lososy, kteří jsou nepříznivě ovlivněni dlouhodobým vystavením vodě obsahující koncentrace NH3 0,006 mg/l. Rovnováha mezi formami NH3 a NH+ 4 závisí na pH (obr. 3).

Rýže. 3. Vliv pH a teploty na distribuci amoniaku a amonných iontů ve vodě
Při pH nižším než 7 je koncentrace NH3 je malý a riziko toxicity je sníženo. Při vyšších hodnotách pH toxicita NH3 zvyšuje. Je třeba poznamenat, že systémy se slanou vodou mají typicky pH 7,5 až 8,3, zatímco sladkovodní systémy mají typicky pH 6,5 až 7,8.
Nitrifikace a bakteriální syntéza produkují vodíkové ionty, takže pH má tendenci klesat během nitrifikace. Ve vodných roztocích jsou vodíkové ionty neutralizovány hydrogenuhličitanovými ionty (C02) ve vodě (při pH nižším než 8,5).
Konečným výsledkem tohoto procesu je snížení koncentrace hydrogenuhličitanu a zvýšení oxidu uhličitého, což obojí přispívá ke snížení pH. K neutralizaci vodíkových iontů vzniklých při oxidaci 1 kg amonia se spotřebuje cca 7,13 kg hydrogenuhličitanu ve formě CaCO6,0. Výpočty beroucí v úvahu rovnováhu kyseliny uhličité ve sladké vodě ukazují, že pokud veškerý oxid uhličitý vzniklý během neutralizace zůstane v roztoku a pH by mělo být vyšší než 0,1, pak je množství amonia (v mg) na litr, které lze oxidovat, přibližně 0 alkality vyjádřené v CaCXNUMX3. Ve většině uzavřených systémů však dochází k částečnému odstranění oxidu uhličitého (například provzdušňováním) a obvykle dochází k určitému snížení pH, takže pravidlo 0,1 zásaditosti poskytuje konzervativní odhad. Uhličitan nebo hydrogenuhličitan je však obvykle nutné přidávat do vody s nízkou alkalitou, aby se pH udrželo na správné úrovni. Toho se často dosahuje použitím uhličitanových hornin jako filtrační vrstvy.
pH systému má také přímý vliv na nitrifikační bakterie. Existují různé názory na vliv pH na rychlost oxidace nitrifikačními bakteriemi. V některých experimentech bylo pozorováno, že rychlost oxidace amonia neadaptovanými kulturami je konstantní pouze při pH 6,8-8. Pod pH 6,8 rychlost oxidace amonia rychle klesá s klesajícím pH. Pro pH nad 8 nebyly provedeny žádné experimenty. V jiných experimentech byla u Nitrosomonas europaea pozorována konstantní rychlost oxidace v rozmezí pH od 7,5 do 9 a u bakterií Nitrosomonas pouze v rozmezí od 8,5 do 8,8. Všechny údaje, s výjimkou posledního, naznačují, že se zdá, že bakterie Nitrosomonas mají nejvyšší a relativně konstantní rychlost oxidace při hodnotách pH mezi 7 a 9. Postupem času se však filtry mohou aklimatizovat na nižší hodnoty pH. Experimenty ukázaly, že 10 dní poté, co bylo pH sníženo na 6, byla bakteriální rychlost oxidace amonného na dusitan rovna rychlosti pozorované při optimálním rozsahu pH. Snížením pH na 5,5 však vznikly podmínky, na které se nitrifikační bakterie nedokázaly adaptovat ani po čase.
Pokud jde o toleranci Nitrobacter, který přeměňuje dusitany na dusičnany, vůči kolísání pH, jsou k dispozici následující informace: Nitrobacter provádí oxidaci nejvyšší rychlostí pouze při pH 8,4 až 9,2. Údaje z čištění domovních odpadních vod ukazují, že optimální oxidační rychlosti byly pozorovány v rozmezí pH od 8,4 do 8,6. Zkušenosti s nitrifikačními filtry v chovu ryb ukazují, že rychlost přeměny dusitanů na dusičnany je dostatečně vysoká, aby udržela přijatelně nízké koncentrace dusitanů při pH 6,5–8,5.
Teplota také ovlivňuje rychlost nitrifikace v biologických filtrech. S klesající teplotou klesá reakční rychlost.
Za předpokladu, že jsou splněny stechiometrické požadavky na kyslík, rychlost nitrifikace nezávisí na koncentraci kyslíku. Při koncentracích kyslíku nižších než stechiometrické požadavky však rychlost reakce rychle klesá (obr. 4).

Rýže. 4. Závislost intenzity nitrifikace na stechiometrické spotřebě kyslíku.
Na základě materiálů od: Wheaton F. Technická podpora pro akvakulturu.















