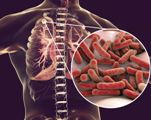
Plicní mykobakterióza je respirační infekce způsobená netuberkulózními druhy mykobakterií. Klinický obraz je charakterizován přítomností bolesti na hrudi, produktivního kašle, dušnosti, hemoptýzy a syndromu intoxikace. Často dochází k infekcím měkkých tkání, kloubů a kostí. Diagnostiku usnadňuje laboratorní identifikace patogenu, histologické a radiologické příznaky. Základem konzervativní léčby plicní mykobakteriózy je vícesložková antibiotická terapie, v některých případech je indikována plicní resekce v různém rozsahu.
ICD-10
A31.0 Plicní infekce způsobená Mycobacterium


- Příčiny
- Charakteristika mikroorganismu
- Infekční mechanismus
- Rizikové skupiny
- Etiotropní terapie
- Patogenetická a symptomatická terapie
- chirurgická léčba
Přehled
Mykobakteriózy jsou oportunní infekce způsobené netuberkulózními (atypickými) mykobakteriemi (NTM). Vyskytují se ve formě lézí podobných tuberkulóze plic, kůže, měkkých tkání, lymfatických uzlin, kloubů a kostí, někdy v diseminované formě. Incidence mykobakteriózy v průmyslových zemích je 1-2:100 000 a stále se zvyšuje. Je to dáno jak zlepšenou diagnostikou, tak nárůstem počtu pacientů s hlubokou imunodeficiencí a imunosupresí. Mykobakterióza je multidisciplinární problém relevantní pro ftizeiopulmonologii, dermatologii a chirurgii.
![Микобактериоз легких]()
Příčiny
Charakteristika mikroorganismu
Rod Mycobacterium sdružuje mykobakterie patogenní (původci lepry, tuberkulózní infekce), oportunní (původci mykobakterióz) a nepatogenní mykobakterie (MB). Mykobakterie jsou tyčinkovité aerobní mikroorganismy odolné vůči kyselinám. Dělí se na rychle rostoucí (tvorí kolonie za méně než 7 dní) a pomalu rostoucí (tvorí kolonie po 7 a více dnech při zachování optimálního prostředí a teploty).
Dosud bylo studováno přes 140 typů netuberkulózních bakterióz s různým stupněm virulence, z nichž asi 40-60 způsobuje mykobakteriózu u lidí. Tyto mikroorganismy jsou všudypřítomné a nacházejí se ve vodě (včetně vodovodní vody) a půdě, některé z nich parazitují na tělech divokých a domácích zvířat a ptáků. Mnoho NTM je odolných vůči dezinfekčním prostředkům a chemoterapeutickým lékům (včetně léků proti tuberkulóze). Z epidemiologického hlediska je největším nebezpečím pro člověka:
- M. avium complex (MAC) – způsobuje plicní mykobakteriózu (až 75 % případů), lymfadenitidu, diseminovanou mykobakteriózu;
- M. kansasii – plicní, generalizovaná mykobakterióza;
- M. Xenopi, M. malmoense – respirační mykobakterióza;
- M. scrofulaceum – mykobakteriální lymfadenitida;
- M. Abscessus, M. Chelonei, M. fortuitum – infekce kůže a měkkých tkání;
- M. ulcerans – vřed Buruli;
- M. marinum – akvarijní/bazénový granulom.
Infekční mechanismus
Studium přenosových cest pro netuberkulózní MB pokračuje. Dnes jsou pravděpodobnými vstupními body pro infekci dýchací trakt, kůže a gastrointestinální trakt. Hlavními mechanismy infekce jsou tedy inhalace, kontakt a fekálně-orální.
Zdrojem infekce jsou domácí zvířata a ptactvo, vodní nádrže (včetně přírodních nádrží, vodovodů, bazénů) a kontaminovaná půda. Nozokomiální šíření infekce je možné při použití dýchacích cest, anestezie, dialyzačních zařízení, intravenózních katétrů, nástrojů a infikovaných transplantátů. Předpokládá se, že infekce zdravého člověka od pacienta je nepravděpodobná, ale existují informace, že přenos infekce z člověka na člověka je relevantní pro HIV infikované osoby s cystickou fibrózou.
Rizikové skupiny
Mykobakterióza postihuje především jedince s narušenou lokální i celkovou imunitou. Respirační mykobakteriální infekce se rozvíjí především u lidí se základním onemocněním, pracujících v nebezpečných odvětvích, pečujících o hospodářská zvířata a starších 50 let. Mezi nejzranitelnější kategorie pro rozvoj plicní mykobakteriózy patří pacienti s následujícími souběžnými patologiemi:
- HIV infekce:
- léková imunosuprese způsobená užíváním cytostatik, kortikosteroidů, monoklonálních protilátek proti TNF-alfa: pacienti s rakovinou, autoimunitními onemocněními, příjemci orgánových a hematopoetických kmenových buněk;
- dysfagie;
- bronchopulmonální onemocnění: COPD, astma, pneumokonióza, sarkoidóza, EBD, tuberkulóza, cystická fibróza;
- celková somatická patologie: diabetes, GERD, srdeční vady;
- narušená produkce endogenního interferonu-gama, IL-12, nedostatek vitaminu D.
Očkování dětí BCG má naopak proti NTM protektivní účinek a vede ke snížení výskytu mykobakteriální lymfadenitidy.
Patogeneze
V rozvoji plicní mykobakteriózy hraje vedoucí roli aerogenní mechanismus infekce, stejně jako reaktivace dormantní infekce. Při vstupu NMB do dýchacího traktu zdravého člověka se aktivují buněčné a humorální obranné mechanismy – fagocytóza, produkce prozánětlivých cytokinů (IFNγ, IL-12, TNF-α), syntéza monocytů a CD4 lymfocytů – díky nimž patogen není eliminován.
U osob s deficitem/defekty imunitního systému se NTM nerušeně množí v dýchacích cestách, usazují se v dýchacích bronchiolech a alveolech, kde se tvoří primární patologické ložisko plicní mykobakteriózy. Odtud NTM proniká do lymfatického řečiště a regionálních lymfatických uzlin a způsobuje fenomén lymfadenitidy.
V další fázi dochází k hematogennímu šíření infekce v plicích s výraznou zánětlivou reakcí, tvorbou epiteloidních obrovskobuněčných granulomů a jevy endobronchitidy a vaskulitidy. Při imunodeficienci se rozvíjí bakteriémie a mykobakteriální infekce generalizuje.
![Микобактериоз легких]()
Klasifikace
Klinická klasifikace plicní mykobakteriózy nebyla vyvinuta. Podle etiologického principu se mykobakterióza rozlišuje v případech HIV, imunosuprese a poruch polykání. V závislosti na převažujících radiologických změnách v klinické pneumologii jsou popsány následující formy:
- Kavitární (kavitární). Častější u starších mužů s CHOPN. V plicích se zjišťují rozpadové dutiny, připomínající ty u tuberkulózy.
- Bronchiektatický. Častěji je detekován u starších žen bez souběžné plicní patologie. Vyznačuje se přítomností broncho- a bronchiolektázy.
- Ohniskové. Charakterizované přítomností solitárních nebo mnohočetných lézí bez klinických příznaků.
Relaps plicní mykobakteriózy je diagnostikován při reaktivaci endogenní infekce a průkazu stejného typu mykobakterií, reinfekce je diagnostikována při absenci bakteriální exkrece během předchozích 10-12 měsíců a následné typizaci nového kmene NTM.
Příznaky plicní mykobakteriózy
Příznaky mykobakteriózy jsou různé a nespecifické. Plicní forma u většiny pacientů připomíná liknavou chronickou infekci dýchacích cest. Nástup onemocnění je často pozvolný (prodromální období může trvat od 1 měsíce do 2 let), méně často – akutní, někdy je mykobakterióza asymptomatická.
Klinický obraz tvoří respirační a intoxikační syndromy. Nejčastějšími stížnostmi pacientů jsou prodloužený, neproduktivní kašel s malým množstvím sputa, epizodická hemoptýza, bolest na hrudi a dušnost. Syndrom intoxikace zahrnuje úbytek hmotnosti, nízkou horečku, hojné noční pocení, bušení srdce a astenie.
Dochází ke zvýšení supra- a podklíčkových lymfatických uzlin. Často je klinický obraz mykobakteriózy superponován projevy doprovodných plicních onemocnění. Infekce MAS je charakterizována stížnostmi na bolesti břicha a průjem.
Komplikace
Poškození dýchacího systému NMB je často komplikováno přidáním plísňové infekce (plicní aspergilóza), tuberkulózy a nozokomiální pneumonie. Na pozadí imunodeficience může být průběh mykobakteriózy generalizován. Extrapulmonální léze se nacházejí ve slezině, játrech, střevech, kostní dřeni a centrálním nervovém systému. Typické je postižení lymfatických uzlin (nitrohrudních, mezenterických, retroperitoneálních) s rozvojem purulentní lymfadenitidy, intraabdominálních a retroperitoneálních abscesů. Časté jsou kožní infekce, abscesy měkkých tkání, purulentní artritida a osteomyelitida.
diagnostika
Diagnostika mykobakterióz je spojena se značnými obtížemi vzhledem k jejich klinické, radiologické a morfologické podobnosti s plicní tuberkulózou. Vedoucí úloha při provádění diagnostických opatření a interpretaci získaných výsledků má pneumolog a ftiziatr. K ověření mykobakteriózy se provádí následující:
- Rentgenová diagnostika. Rentgenové nebo CT vyšetření plic obvykle zobrazuje oboustranné rozpadové dutiny, infiltrativní ložiska nebo bronchiektázie (někdy jsou zaznamenány kombinované změny). Mezi doprovodné změny patří deformace plicního vzoru, zvýšení VLN, kalcifikace, bulózní emfyzém atd.
- Kulturní výzkum. Na živných médiích se provádí 3násobná kultivace sputa, pokud není možné získat sputum, vyšetřují se výplachy průdušek. Etiologická diagnóza se považuje za potvrzenou, když je kultivace z výplachové tekutiny jednou pozitivní nebo kultivace sputa je dvakrát pozitivní. Pro výběr léčebného režimu je také důležité stanovení lékové citlivosti a druhové identifikace NMB, která se provádí pomocí PCR.
- Biopsie. V závislosti na klinické situaci se vzorky tkáně odebírají během bronchoskopie, biopsie lymfatických uzlin, diagnostické mediastinoskopie nebo torakoskopie. Přítomnost granulomatózního zánětu nebo acidorezistentní NMB svědčí pro plicní mykobakteriózu.
- Tuberkulínové testy. Role testu Mantoux v diagnostice plicní mykobakteriózy zůstává kontroverzní. Jeho negativní výsledek však s vysokou pravděpodobností vyloučí tuberkulózní infekci.
- Hematologické studie. U pacientů s verifikovanou mykobakteriózou je nutné stanovit HIV status, stav buněčné (T-lymfocyty, B-lymfocyty) a humorální (imunoglobuliny tříd A, G, M) imunity. Pro posouzení aktivity zánětlivého procesu se vyšetřují CBC s počtem leukocytů a ESR, markery akutní fáze.
![Рентген легких при микобактериозе]()
Rentgenový snímek plic s mykobakteriózou
Léčba plicní mykobakteriózy
Etiotropní terapie
Stanovení indikací pro antibiotickou terapii je další kontroverzní otázkou ve studiu mykobakterióz. Předpokládá se, že v asymptomatických případech není léčba nutná, protože NMB jsou oportunní patogeny. Podle řady vědců je třeba k této problematice přistupovat individuálně s ohledem na věk pacienta, doprovodná onemocnění a rentgenový snímek.
Při předepisování antibiotické terapie se volí ve prospěch vícesložkových režimů, parenterálního podávání léků a dlouhých kurzů. Výběr antibiotika se provádí s ohledem na typ patogenu:
- naMAC infekce: makrolidy, antituberkulotika, aminoglykosidy;
- naM.kansasii: antituberkulózní antibiotika, makrolidy, sulfonamidy, aminoglykosidy, fluorochinolony;
- naM.xenopi: ansamyciny, makrolidy, fluorochinolony, aminoglykosidy;
- naM.fortuitum: fluorochinolony, sulfonamidy, makrolidy, aminoglykosidy, cefalosporiny;
- naM.fortuitum,M.absces: tetracykliny, karbapenemy atd.
Patogenetická a symptomatická terapie
Doporučuje se přestat kouřit a jíst výživnou stravu. Patogenetická léčba zahrnuje předepisování bronchodilatancií (perorální, inhalační, nebulizační terapie), mukoaktivních, imunotropních léků. Pokud je drenážní funkce bronchiálního stromu neuspokojivá, je indikována sanitární bronchoskopie.
Ke snížení zánětlivého procesu mohou být indikovány NSAID, glukokortikoidy, vitamíny, protidestičkové látky a antioxidanty. Mezi nedrogová opatření patří dechová cvičení, perkusní masáže, oxygenoterapie a fyzioterapeutické procedury.
chirurgická léčba
Pokud je radikální sanitace dýchacích cest nemožná a jsou přítomny přetrvávající morfologické změny v plicích, vyvstává otázka chirurgických metod léčby mykobakteriózy. Rozsah plicní resekce může být variabilní: od klínové excize, segmentové a lobektomie až po pneumonektomii a pleuropneumonektomii. Předoperační a pooperační antimikrobiální chemoterapie je povinná. Po ukončení léčby se doporučuje mikrobiologické a radiologické sledování po dobu jednoho roku.
Prognóza a prevence
Mykobakterióza je potenciálně smrtelné onemocnění, zejména pro imunokompromitované pacienty. Úmrtnost v této skupině je 14 %. Léčba se provádí v dlouhých cyklech (12 až 24 měsíců), komplikovaných lékovou rezistencí mykobakterií a obtížemi při výběru racionálního režimu antibiotické terapie. Často je vyžadována kombinace konzervativní a chirurgické taktiky.
U řady léčených pacientů dochází během následujících 5 let k relapsům mykobakteriózy, takže tito pacienti vyžadují dlouhodobé, někdy celoživotní sledování. Vzhledem k tomu, že onemocnění se nejčastěji vyskytuje u pacientů s imunodeficiencí a doprovodnými patologiemi dýchacího systému, je nutné dbát na prevenci těchto patologií. Ve zdravotnických zařízeních je nutné provádět protiepidemická opatření a sledovat zdravotní stav pracovníků v nebezpečných odvětvích.
1. Mykobakterióza dýchacího systému v moderní ftizeiopulmonologické praxi: diagnostika, klinický obraz, léčba a pozorování. Disertační práce / Guntupová L. D. – 2020.
2. Epidemiologické rysy mykobakteriózy způsobené netuberkulózními mykobakteriemi/ Solomay T.V.// Hygienický lékař. – 2015. – č. 3.
3. Mykobakterióza v praxi pneumologa: stav problému / Shmelev E.I., Kovalevskaya M.N., Ergeshov A.E., Chernousova L.N., Larionova E.E.// Praktická pulmonologie. – 2016.
4. Mykobakterióza ve ftizeiopulmonologické praxi: přehled literatury a osobní zkušenosti/ Guntupova L.D., Borisov S.E., Solovyova I.P., Makarova M.V., Chačaturyants E.N.
















