Malachitová zeleň je organická sloučenina, která se používá jako barvivo a je známá jako antimikrobiální látka v akvakultuře. Malachitová zeleň se tradičně používá jako barvivo pro materiály, jako je hedvábí, kůže a papír. Navzdory svému názvu není barvivo vyrobeno z minerálu malachit a název pochází z podobnosti barvy.
- 1 Struktury a vlastnosti
- 2 Příprava
- 3 Použití
- 3.1 Specifické použití
Struktura a vlastnosti
Malachitová zeleň je v průmyslu barviv klasifikována jako triarylmethanové barvivo a používá se také v průmyslu pigmentů. Formálně malachitová zeleň odkazuje na chloridovou sůl [C6H5C(C6H4N(CH3)2)2]Cl), ačkoli termín malachitová zeleň se používá volně a často jednoduše odkazuje na barevný kation. Na trhu je k dostání i šťavelanová sůl. Anionty neovlivňují barvu. Intenzivní zelená barva kationtu je výsledkem silného absorpčního pásu při 621 nm (extinkční koeficient 10 milionů cm ).
Malachitová zeleň (druhý přechod) (indikátor pH) pH pod 11,5 nad pH 13,2 11,5 ⇌ 13,2 Malachitová zeleň (první přechod) (indikátor pH) pH pod 0,2 nad pH 1,8 0,2 ⇌ 1,8 Malachitová zeleň se připravuje kondenzací benzaldehydu a dimethylanilinu za vzniku leuko malachitové zeleně (LMG):
C6H5CHO + 2 C 6H5N (CH 3) 2 → C 6H5CH (C 6H4N (CH 3) 2) 2+ H 2O
Za druhé, tato bezbarvá leukosloučenina, příbuzná trifenylmethanu, se oxiduje na kation, kterým je MG:
C6H5CH (C 6H4N (CH 3) 2) 2+ HCl + ⁄ 2O2 → [C 6H5C (C 6H4N (CH 3) 2) 2] Cl + H 2O
![]()
Vlevo je leukomalachitová zeleň (LMG) a vpravo dvě ekvivalentní rezonanční struktury kationtu MG. Alkoholový derivát MG se připravuje z LMG nahrazením jedinečného C–H za C–OH.
Hydrolýzou MG vzniká alkohol:
[C6H5C (C 6H4N (CH 3) 2) 2] Cl + H 2O → C 6H5C (OH) (C 6H4N (CH 3) 2) 2+ HCl
) Tento alkohol je důležitý, protože on, a ne MG, proniká buněčnými membránami. Jakmile je uvnitř buňky, je metabolizován na LMG. Pouze kationt MG je hluboce zbarven, zatímco leuko- a alkoholové deriváty nikoli. Tento rozdíl vzniká, protože pouze kationtová forma má rozšířenou pi-delokalizaci, která umožňuje molekule absorbovat viditelné světlo.
Příjem
Forma leuko malachitové zeleně byla poprvé připravena Hermannem Fischerem v roce 1877 kondenzací benzaldehydu a dimethylanilinu v molekulárním poměru 1:2 v přítomnosti kyseliny sírové.
![Синтез малахитового зеленого]()
Použití
Malachitová zeleň se tradičně používá jako barvivo. Pro tento účel se ročně vyrobí kilotuny MG a příbuzných triarylmethanových barviv.
MG je opět aktivní v oomycetě Saprolegnia, která napadá rybí jikry v komerční akvakultuře, MG se používá k léčbě Saprolegnie a používá se jako antibakteriální. Jedná se o velmi oblíbený prostředek proti Ichthyophthirius multifiliis ve sladkovodních akváriích. Hlavní metabolit, LMG, se nachází v rybách ošetřených malachitovou zelení, což je objev, který byl základem kontroverze a vládní regulace. Viz také Antimikrobiální látky v akvakultuře.
MG bylo často používáno k chytání zlodějů a zlodějů. Návnada, obvykle peněžní návnada, je posypána bezvodým práškem. Každý, kdo manipuluje s kontaminovanými penězi, zjistí, že po umytí rukou se na kůži vytvoří zelená skvrna, která vydrží několik dní.
Niche používá
![]()
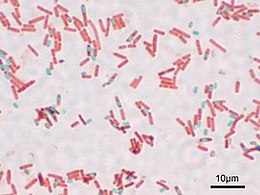
preparát Bacillus subtilis vykazující endospory obarvené malachitovou zelení (vegetativní buňky obarvené růžově safraninovým kontrastním barvivem)
Mnoho specializovaných aplikací používá intenzivní barvu MG. Používá se jako biologické barvivo pro mikroskopickou analýzu buněčné biologie a vzorků tkání. Při metodě barvení Gimenez základní fuchsin barví bakterie červeně nebo fialově a jako modrozelené kontrastní barvivo se používá malachitová zeleň. Malachitová zeleň se také používá k barvení endospor, protože může přímo barvit endospory uvnitř bakteriálních buněk; často se zde používá kontrastní barvivo safranin. Malachitová zeleň je součástí pylové skvrny Alexandra. Malachitovou zeleň lze také použít jako saturovatelný absorbér v barvivových laserech nebo jako indikátor pH v rozmezí pH 0,2–1,8. Takové použití je však poměrně vzácné. Leukomalachitová zeleň (LMG) se používá jako metoda pro detekci okultní krve ve forenzní vědě. Hemoglobin katalyzuje reakci mezi LMG a peroxidem vodíku a mění bezbarvý LMG na malachitovou zeleň. Vzhled zelené barvy tedy naznačuje přítomnost krve.
Dekret
V roce 1992 kanadské úřady určily, že konzumace ryb kontaminovaných malachitovou zelení představuje významné zdravotní riziko. Malachitová zeleň byla klasifikována jako zdravotní riziko třídy II. Kvůli nízkým výrobním nákladům se malachitová zeleň stále používá v některých zemích s méně přísnými zákony pro účely mimo akvakulturu. V roce 2005 našli analytici v Hong Kongu stopy malachitové zeleně u úhořů a ryb dovezených z Číny a Tchaj-wanu. V roce 2006 našel americký Úřad pro kontrolu potravin a léčiv (FDA) malachitovou zeleň v mořských plodech dovezených mimo jiné z Číny, kde je použití této látky také zakázáno v akvakultuře. V červnu 2007 FDA zablokoval dovoz několika druhů mořských plodů kvůli pokračující kontaminaci malachitovou zelení. Látka je ve Spojených státech zakázána od roku 1983 pro potravinářské použití. Ve Spojeném království je také zakázáno. Zvířata metabolizují malachitovou zeleň na její leuko formu. Protože je lipofilní (leukoforma má log P 5,70), setrvává metabolit ve svalovině sumce déle (HL = 10 dní) než mateřská molekula (HL = 2,8 dne).
Toxicita
LD50 (orálně, myš) je 80 mg/kg. U potkanů léčených malachitovou zelení došlo k „dávkově závislému zvýšení aduktů DNA v játrech spolu s plicními adenomy. Leukomalachitová zelená způsobuje „nárůst počtu a závažnosti změn“. Protože leukomalachitová zeleň je hlavním metabolitem malachitové zeleně a přetrvává mnohem déle ve svalovině ryb, většina lidí konzumujících malachitovou zeleň v důsledku konzumace ryb bude ve formě leukocytů. Během experimentu bylo potkanům podáno až 543 ppm leukomalachitové zeleně, což je nadměrné množství ve srovnání s průměrem 5 ppb nalezeným v rybách. Po dvou letech bylo u samců potkanů zjištěno zvýšení počtu plicních adenomů, ale nebyly zaznamenány žádné případy jaterních nádorů. Lze tedy učinit závěr, že malachitová zeleň způsobuje karcinogenní příznaky, ale přímá souvislost mezi malachitovou zelení a nádory jater nebyla prokázána.
Objev
Ačkoli malachitová zeleň ve vodném roztoku prakticky nefluoreskovala (kvantový výtěžek 7,9×10), několik výzkumných skupin vyvinulo technologie k detekci malachitové zeleně. Například Zhao a kol. Prokázalo použití aptameru malachitové zeleně v mikrokonzolových senzorech k detekci nízkých koncentrací malachitové zeleně.
reference
další literatura
- Cho, Bongsup P.; Yang, Tianle; Blankenship, Lonnie R.; a další. (2003). „Syntéza a charakterizace N-demethylovaných metabolitů malachitové zeleně a leukomalachitové zeleně“. Chem. Res. Toxicol. 16(3):285–294. doi:10.1021/tx0256679. PMID12641428.
- Plakas, S.M.; El Said, K.R.; Stehly, G. R.; a další. (1996). „Absorpce, distribuce v tkáních a metabolismus sumce malachitového zeleného kanálu (Ictalurus punctatus)“. Možná. J. Fish. Aquat. Sci. 53(6):1427–1433. doi:10.1139/cjfas-53-6-1427.
- Schoettger, 1970; Smith a Heath, 1979; Gluth a Hanke, 1983. Bills a kol. (1977)
- DeFina, Stephen K.; Dieckmann, Torsten (2002). „Syntéza selektivně N- nebo C-značené malachitové zeleně“. Journal of Labeled Compounds and Radiopharmaceuticals. 45(3):241–248. doi:10.1002/jlcr.554.
- Dhamgaye, S; Devaux, F; Manoharlal, R; a další. (leden 2012). “Účinek malachitové zeleně na Candida albicans in vitro zahrnuje více drah a transkripčních regulátorů UPC2 a STP2.” Antimikrobiální látky Chemother. 56(1):495–506. DOI: 10.1128/AAC.00574-11. PMC3256066. PMID22006003.
externí odkazy
Wikimedia Commons má materiál související s malachitovou zelení. - USA. Národní institut zdraví
- US Food and Drug Administration
- Ministerstvo zdravotnictví Spojeného království
- Malachitová zeleň – metoda barvení endospor (video)
Tento článek je o organickém barvivu zvaném malachitová zeleň. Pro použití malachitu jako pigmentu viz Malachit, § Použití a základní uhličitan měďnatý, § Použití.
![Малахитовый зеленый оксалат.jpg]()
Jména Název IUPAC 4 — — N , N- Dimethylcyklohexa-2,5-dien-1-iminiumchlorid
Anilinová zelená; Základní zelená 4; Diamantová zelená B; Viktoria zelená B- 569-64-2 (chloridová sůl) Y
- 2437-29-8 (oxalátová sůl) N
- ChEMBL186357 Y
- 10820 Y
- 12058M7ORO Y
- DTXSID1025512
InChI = 1S / C23H25N2.ClH / cl-1 (24) 2-21-14-10 (19-11-15) 21 (23-18-8-6-5-7-9) 18-20-12- 16 (22-17-13) 20 (25) 3; /h4-5H, 17-1H4; 3H/q + 1; / p-1 Y
Klíč: FDZZZRQASAIRJF-UHFFFAOYSA-M Y
InChI = 1 / C23H25N2.ClH / cl-1 (24) 2-21-14-10 (19-11-15) 21 (23-18-8-6-5-7-9) 18-20-12- 16 (22-17-13) 20 (25) 3; /h4-5H, 17-1H4; 3H/q + 1; /p-1
Klíč: FDZZZRQASAIRJF-REWHXWOFAA
CN (C) c1ccc (cc1) C (= C2C = CC (= [N +] (C) C) C = C2) c3cccc3. [Cl-]Pokud není uvedeno jinak, údaje platí pro materiály v jejich standardním stavu (při 25 °C [77 °F], 100 kPa).
Malachitová zeleň je organická sloučenina, která se používá v akvakultuře jako barvivo a je známá jako antimikrobiální činidlo. Malachitová zeleň se tradičně používá jako barvivo pro materiály, jako je hedvábí, kůže a papír. Navzdory svému názvu není barvivo vyrobeno z minerálu malachit a název pochází z podobnosti barev.
- 1 Struktury a vlastnosti
- 2 Příprava
- 3 použití
- 3.1 Použití výklenku
Struktury a vlastnosti[editovat]
Malachitová zeleň je v průmyslu barviv klasifikována jako triarylmethanové barvivo a používá se také v průmyslu pigmentů. Formálně malachitová zeleň označuje chloridovou sůl [C 6 H 5 C(C 6 H 4 N(CH 3 ) 2 ) 2 ]Cl, ačkoli termín “malachitová zeleň” se používá volně a často se jednoduše vztahuje k barevnému kationtu. Prodává se také šťavelanová sůl. Anionty nemají žádný vliv na barvu. Intenzivní zelená barva je výsledkem kationtů ze silného absorpčního pásu při 621 nm (extinkční koeficient 10 5 M−1 cm−1).
Malachitová zelená (druhý přechod) (ukazatel pH) pH pod 11,5 nad pH 13,2 11,5 ⇌ 13,2 Malachitová zelená (první přechod) (ukazatel pH) pH pod 0,2 nad pH 1,8 0,2 ⇌ 1,8 Malachitová zeleň se vyrábí kondenzací benzaldehydu a dimethylanilinu za vzniku leukomalachitové zeleně (LMG):
Za druhé, tato bezbarvá leukosloučenina, příbuzná trifenylmethanu, se oxiduje na kationt MG:
Typickým oxidačním činidlem je oxid manganičitý.
Vlevo je leukomalachitová zeleň (LMG) a vpravo dvě ekvivalentní rezonanční struktury kationtu MG. Alkoholový derivát MG se připravuje z LMG nahrazením jedinečného C–H za C–OH.
Hydrolýzou MG vzniká alkohol: [1]
Tento alkohol je důležitý, protože on, a ne MG, proniká buněčnými membránami. Jakmile je uvnitř buňky, je metabolizován na LMG. Pouze kationt MG je hluboce zbarven, zatímco deriváty leukocytů a alkoholu nikoli. Tento rozdíl vzniká, protože pouze kationtová forma má rozšířenou pi-delokalizaci, která umožňuje molekule absorbovat viditelné světlo.
příprava[editovat]
Leuko formu malachitové zeleně poprvé připravil Hermann Fischer v roce 1877 kondenzací benzaldehydu a dimethylanilinu v molekulárním poměru 1:2 v přítomnosti kyseliny sírové. [2]
Používá [upravit]
Malachitová zeleň se tradičně používá jako barvivo. Za tímto účelem se ročně vyrobí kilotuny MG a příbuzných triarylmethanových barviv. [3]
MG je aktivní proti oomycete Saprolegnie , který ovlivňuje jikry v komerční akvakultuře. MG se používá k léčbě Saprolegnie a jako antibakteriální činidlo. [4] Jedná se o velmi oblíbený prostředek proti Ichthyophthirius multifiliis ve sladkovodních akváriích. Hlavní metabolit LMG se nachází v rybách ošetřených malachitovou zelení a tento objev je základem kontroverzí a vládních nařízení. Viz také Antimikrobiální látky v akvakultuře.
MG bylo často používáno k chytání zlodějů a zlodějů. Návnada, obvykle peněžní návnada, je posypána bezvodým práškem. Každý, kdo manipuluje s kontaminovanými penězi, zjistí, že po umytí rukou se na kůži vytvoří zelená skvrna, která vydrží několik dní. [ cenová nabídka nutná ]
Nisha používá[editovat]
Příprava Bacillus subtilis s endosporami obarvenými malachitovou zelení (vegetativní buňky obarvené růžově safraninovým kontrastním barvivem)
Intenzivní barva MG se používá v mnoha specializovaných aplikacích. Používá se jako biologické barvivo pro mikroskopickou analýzu buněčné biologie a vzorků tkání. Při metodě barvení Gimenez základní fuchsin barví bakterie červeně nebo fialově a jako modrozelené kontrastní barvivo se používá malachitová zeleň. Malachitová zeleň se také používá k barvení endospor, protože může přímo barvit endospory v bakteriálních buňkách; zde se často používá safraninové kontrastní barvivo. Malachitová zeleň je součástí pylové skvrny Alexandra. Malachitovou zeleň lze také použít jako saturovatelný absorbér v barvivových laserech nebo jako indikátor pH v rozmezí pH 0,2–1,8. Takové použití je však poměrně vzácné. Leukomalachitová zeleň (LMG) se používá jako metoda pro detekci okultní krve ve forenzní vědě. Hemoglobin katalyzuje reakci mezi LMG a peroxidem vodíku a mění bezbarvý LMG na malachitovou zeleň. Proto vzhled zelené barvy naznačuje přítomnost krve. [5]
Pravidla [editovat]
V roce 1992 kanadské úřady určily, že konzumace ryb kontaminovaných malachitovou zelení představuje významné zdravotní riziko. [6] Malachitová zeleň byla klasifikována jako zdravotní riziko třídy II. Kvůli nízkým výrobním nákladům se malachitová zeleň stále používá v některých zemích s méně přísnými zákony pro neakvakulturu. V roce 2005 našli analytici v Hong Kongu stopy malachitové zeleně u úhořů a ryb dovezených z Číny a Tchaj-wanu. V roce 2006 objevil americký Úřad pro kontrolu potravin a léčiv (FDA) malachitovou zeleň v mořských plodech dovážených mimo jiné z Číny, kde je použití této látky také zakázáno v akvakultuře. V červnu 2007 FDA zablokoval dovoz několika druhů mořských plodů kvůli pokračující kontaminaci malachitovou zelení. [7] Látka je ve Spojených státech zakázána pro použití v potravinách od roku 1983. Ve Spojeném království je také zakázáno. [8] Zvířata metabolizují malachitovou zeleň na leuko formu. Vzhledem k tomu, že je metabolit lipofilní (leukoforma má log P 5,70), setrvává ve svalovině sumce déle (HL = 10 dní) než mateřská molekula (HL = 2,8 dne).
Toxicita[editovat]
LD50 (orálně, myš) je 80 mg/kg. [ cenová nabídka nutná ] U potkanů krmených malachitovou zelení došlo k „dávce závislému zvýšení aduktů jaterní DNA“ spolu s plicními adenomy. Leukomalachitová zelená způsobuje „nárůst počtu a závažnosti změn“. Protože leukomalachitová zeleň je hlavním metabolitem malachitové zeleně a přetrvává mnohem déle ve svalovině ryb, většina lidí konzumujících malachitovou zeleň v důsledku konzumace ryb bude ve formě leukocytů. Během experimentu bylo potkanům podáno až 543 ppm leukomalachitové zeleně, což je extrémní množství ve srovnání s průměrem 5 ppb nalezeným v rybách. Po dvou letech bylo u samců potkanů zjištěno zvýšení počtu plicních adenomů, ale nevyskytly se žádné případy nádorů jater. Lze tedy učinit závěr, že malachitová zeleň způsobuje karcinogenní příznaky, ale přímá souvislost mezi malachitovou zelení a nádory jater nebyla prokázána. [9]
objev[editovat]
Ačkoli malachitová zeleň nemá ve vodném roztoku téměř žádnou fluorescenci (kvantový výtěžek 7,9 × 10−5), [10] několik výzkumných skupin vyvinulo technologie pro detekci malachitové zeleně. Například Zhao a kol. Prokázalo použití aptameru malachitové zeleně v mikrokonzolových senzorech k detekci nízkých koncentrací malachitové zeleně. [jedenáct]
Odkazy [upravit]
- ^ Adina Raducan, Alexandra Olteanu, Mihaela Puiu, Dumitru Oancea „Vliv povrchově aktivních látek na vyblednutí malachitové zeleně“ Central – European Journal of Chemistry , 2008, ročník 6, s. 1895-1066 (Tisk) 1644-3624 (Online). DOI: 10,2478/s11532-007-0066-0
- ^ Dr. M. Viswanathan. Základy organické chemie . Publikace Jai Sai. S. 2/37.
- ^ Thomas Gessner a Udo Mayer „Triarylmethanová a diarylmethanová barviva“ v Ullmanova encyklopedie průmyslové chemie 2002, Wiley-VCH, Weinheim. DOI: 10.1002/14356007.a27_179
- ^ Srivastava, S; Sinha, R; Roy, D. (2004). „Toxikologické účinky malachitové zeleně“. Vodní toxikologie . 66 (3): 319–29. DOI: 10.1016/j.aquatox.2003.09.008. PMID 15129773.
- ^ „Tréninkový protokol pro laboratorní školení DNA analytiků 2.18. Navrhovaný leukomalachitový zelený krevní test“ (PDF). Národní centrum forenzních technologií. Staženo 8. ledna 2018.
- ^ Wendy K. Andersen, Sherry B. Repa a Jose E. Roybal “Kvantitativní a potvrzující analýza zbytků malachitové zeleně a leukomalachitové zeleně v rybách a krevetách” J. Agric. Food Chem. 2006, ročník 54, s. 4517–4523. doi:10.1021/jf0532258 a odkazy v něm uvedené
- ^ Čínská rybářská krize odhaluje problémy s bezpečností mořských plodů. USA Today , 01.07.2007
- ^ Výbor pro veterinární rezidua. Výroční zpráva o sledování veterinárních reziduí v potravinách ve Spojeném království za roky 2001, 2002 a 2003. Archivováno 11. února 2012 na Wayback Machine.
- ^ Culp, S.J.; Beland, F. A.; Heflich, R. H.; a další. (2002). „Mutagenita a karcinogenita týkající se tvorby aduktů DNA u potkanů léčených leukomalachitovou zelení“. Mutační studie . 506–507: 55–63. DOI: 10.1016/S0027-5107(02)00152-5. PMID 12351145.
- ^ Babendure, Jeremy R.; Adams, Stephen R.; Tsien, Roger Y. (2003). “Aptamery zapínají fluorescenci trifenylmethanových barviv.” Journal of the American Chemical Society . Americká chemická společnost (ACS). 125 (48): 14716–14717. DOI: 10.1021/ja037994o. ISSN 0002-7863. PMID 14640641.
- ^ Vliv připojení receptoru na citlivost mikrokonzolového biosenzoru bez označení pomocí malachitově zeleného aptameru https://doi.org/10.1016/j.snb.2019.126963
Další čtení[editovat]
- Cho, Bongsup P.; Yang, Tianle; Blankenship, Lonnie R.; a další. (2003). „Syntéza a charakterizace N-demethylovaných metabolitů malachitové zeleně a leukomalachitové zeleně“. Chem. Res. Toxicol . 16 (3): 285–294. DOI: 10.1021/tx0256679. PMID 12641428.
- Plakas, S.M.; El Said, KR; Stehly, G. R.; a další. (1996). “Absorpce, distribuce v tkáních a metabolismus malachitového zeleného kanálového sumce ( Ictalurus punctatus ) ». Možná. J. Fish. Aquat. Sci . 53 (6): 1427–1433. DOI: 10.1139/cjfas-53-6-1427.
- Schoettger, 1970; Smith a Heath, 1979; Gluth a Hanke, 1983. Bills et al. (1977)
- DeFina, Stephen S.; Dieckmann, Torsten (2002). „Syntéza selektivně 15N nebo 13C značené malachitové zeleně“. Journal of Labeled Compounds and Radiopharmaceuticals . 45 (3): 241–248. DOI: 10.1002/jlcr.554.
- Dhamgaye, S; Devaux, F; Manoharlal, R; a další. (leden 2012). „Účinky malachitové zeleně na Candida albicans in vitro zahrnují více drah a transkripčních regulátorů UPC2 a STP2“. Chemother Antimikrobiální činidla . 56 (1): 495–506. DOI: 10,1128/AAC.00574-11. PMC 3256066. PMID 22006003.
Externí odkazy[editovat]
Wikimedia Commons má související média malachitová zeleň . - US National Institutes of Health
- US Food and Drug Administration
- Ministerstvo zdravotnictví Spojeného království
- Malachitová zeleň – technika barvení endospor (video)